News - ¿Cómo aparecen en el mercado los medicamentos no registrados?
Business Strategy
¿Cómo aparecen en el mercado los medicamentos no registrados?
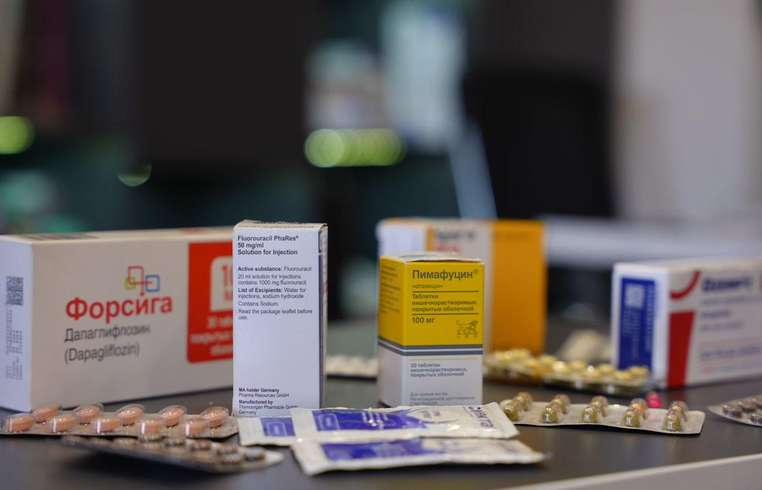
En Armenia, muchos medicamentos recetados para el cáncer, la diabetes, trastornos hormonales y otras enfermedades no están registrados y, por lo tanto, no pueden venderse legalmente. Sin embargo, estos medicamentos se venden libremente en farmacias o en el mercado negro. Debido a que no están registrados, ningún órgano estatal comprueba su eficacia y seguridad. Durante años, los médicos han advertido que estos medicamentos son imprescindibles para sus pacientes y deberían estar registrados y debidamente probados para evitar que circulen medicamentos falsificados, pero el estado no ha logrado resolver el problema del registro. Hetq obtuvo de las sucursales urbanas y regionales de una cadena de farmacias de Yereván 13 medicamentos que no cuentan con registro legal en Armenia. No mencionamos la cadena para evitar señalar a una empresa en particular, ya que es posible que estos medicamentos se vendan también en otras cadenas. Por qué muchos medicamentos importantes no están registrados en Armenia El proceso de registro de fármacos en Armenia es largo y costoso. Según el Ministerio de Salud, actualmente hay 3.661 nombres de medicamentos registrados en Armenia. Marine Harutyunyan, jefa del Departamento de Política de Medicamentos y Tecnologías Médicas, dice que a veces algunos medicamentos no llegan a Armenia no por restricciones estatales, sino por falta de interés de los fabricantes. Antes de registrar un fármaco, se realizan numerosos estudios, tanto documentales como de laboratorio. Si los resultados son positivos, el fármaco se registra mediante una orden ministerial por un plazo de cinco años. Harutyunyan señala que el mercado farmacéutico de Armenia es pequeño, por lo que algunos fabricantes no solicitan el registro de los fármacos. El registrante puede ser el titular del fármaco o el fabricante, lo que significa que los documentos necesarios deben ser proporcionados y ser de propiedad del fabricante o de los titulares de derechos autorizados. Dado el pequeño tamaño del mercado, a menudo no surge el interés de los fabricantes. Según Harutyunyan, los rechazos no obedecen a una decisión personal de un ministro o de un experto. Los rechazos están claramente definidos por la ley y por actos subreglamentarios. Si hay una conclusión negativa, como resultados de laboratorio insatisfactorios o deficiencias documentales, y si estos problemas no se corrigen dentro de 180 días, se deniega el registro de conformidad con los requisitos legales. Con respecto a los medicamentos que llegan a Armenia a través de canales ilegales, Harutyunyan dice que el problema proviene de los intereses de los fabricantes. Si un fabricante no solicita el registro en nuestro país, el Estado no puede obligarlo. Pero se han introducido cambios legislativos y existe una lista de medicamentos esenciales. Si un fármaco o una forma farmacéutica figura en esa lista, su importación está permitida por orden ministerial tras revisión documental. El mercado negro de medicamentos no está bajo el control del Ministerio de Salud. El ministerio no tiene poderes de supervisión; la supervisión corresponde a la Inspección Estatal de Salud y Trabajo, que realiza comprobaciones casi a diario. Si se registra la venta de un medicamento no registrado, se imponen sanciones y multas severas. Para importar medicamentos, una organización debe estar licenciada, contar con almacenes y personal cualificado. Durante la importación, la documentación es revisada por las autoridades aduaneras y un centro de expertos. El proceso toma de 7 a 10 días hábiles, tras los cuales se emite una conclusión positiva o negativa. Harutyunyan enfatiza que los medicamentos importados legalmente que no están registrados suelen ser esenciales. Se refieren únicamente a importaciones legales. La adquisición a través de compras estatales está permitida no solo para los ministerios de Salud y Defensa, sino también para las instituciones médicas. Sin embargo, todos los medicamentos no registrados deben ser fabricados y registrados en los países miembros de la Unión Económica Eurasiática (UEEA). La importación de medicamentos no registrados desde otros países no está permitida. No obstante, las farmacias armenias venden medicamentos que no son producidos por países miembros de la UEEA, ni han llegado a Armenia a través de canales autorizados con permiso ministerial. ¿Se supervisa adecuadamente la venta de medicamentos no registrados en Armenia? Harutyunyan responde que no puede evaluarlo porque esa función no es competencia del ministerio. Pero existen actos legales y regulatorios claros que rigen la supervisión y, hasta donde saben, la supervisión se lleva a cabo. Cómo se venden los medicamentos en las farmacias Hetq obtuvo los siguientes medicamentos: - Ozempic 0,5 mg (lote PP5N094, caducidad mayo de 2027, comprado 26 de agosto de 2025). El medicamento se vendió sin la etiqueta de sello y con recibo fiscal. - Tegretol 200 mg (lote TLHW5, caducidad enero de 2027, comprado 24 de julio de 2025). Tanto el recibo fiscal como la etiqueta de sello estaban presentes. - Forsiga 10 mg (lote 2720325, caducidad febrero de 2028, comprado 1 de agosto de 2025). El recibo fiscal y la etiqueta de sello estaban presentes. - Pimafucin 100 mg tabletas (lote 020290, caducidad octubre de 2027, comprado 23 de julio de 2025). El recibo fiscal y la etiqueta de sello estaban presentes. - Baralgin (lote 4P0563A, caducidad enero de 2028, comprado 23 de julio de 2025). El recibo fiscal y la etiqueta de sello estaban presentes. Del dato en las etiquetas de la caja se dedujo que el importador introdujo en el registro de etiquetas un código que no tenía relación con el fármaco. En lugar del código ATC/HS correcto (3004), se introdujo un código de vitamina sin envase (2936). Este producto analgésico y antipirético también figura como vitamina no certificada. - Omnic (lote 571124, caducidad julio de 2028, comprado 23 de julio de 2025). El recibo fiscal está presente, pero falta la etiqueta de sello. - Vesicar (lote 154378, caducidad abril de 2026, comprado 23 de julio de 2025). Se vendió sin recibo fiscal y sin etiqueta de sello. - Allohol (Pharmstandard, lote 740524, caducidad abril de 2028, comprado 23 de julio de 2025). El recibo fiscal está presente, pero falta la etiqueta de sello. - Smecta (lote C56167, caducidad abril de 2027, comprado 23 de julio de 2025). El recibo fiscal está presente, pero falta la etiqueta de sello. - Attarax (lote 409451, caducidad junio de 2029, comprado 23 de julio de 2025). El recibo fiscal está presente, pero falta la etiqueta de sello. - Senade (lote 484007, caducidad abril de 2027, comprado 22 de julio de 2025). El recibo fiscal está presente, pero falta la etiqueta de sello. 12–13. Xeloda (lote 2408547, caducidad junio de 2027) y Fluorouracil 50 mg/ml (PhaRes, Alemania, lote 440700, caducidad junio de 2026) se adquirieron el 12 de agosto de 2025. El recibo fiscal está presente, pero falta la etiqueta de sello. Hetq envió la lista de medicamentos que compró al Ministerio de Salud y preguntó cuáles de ellos estaban certificados. El ministerio respondió que, entre los 13 medicamentos no registrados, solo Tegretol, la versión italiana, tenía un certificado de importación emitido. En el caso de Pimafucin, el ministerio rechazó la solicitud de la empresa, pero eso no impide la venta. Para los otros 12 medicamentos, el ministerio no presentó ninguna solicitud en su sistema de Documentos de Autorización. Sin embargo, estos medicamentos están disponibles en la cadena de farmacias que visitamos. Las pruebas de registro de fármacos las realiza el Centro de Medicamentos y Tecnologías Médicas del Ministerio de Salud. Según la subdirectora del centro, Naira Romanyova, los medicamentos en Armenia se registran mediante procedimientos generales y simplificados, así como de acuerdo con las normas de la Unión Económica Euroasiática (UEEA). El procedimiento simplificado se aplica a fármacos registrados en países miembros de organizaciones profesionales internacionales designadas por el gobierno o a fármacos que ya están pre‑calificados por las normas de la Unión Económica Euroasiática (UEEA). El plazo de registro de fármacos depende del procedimiento: el registro nacional simplificado toma 31 días, el registro general hasta 150 días y el registro en la UEEA hasta 180 días hábiles. Las empresas farmacéuticas deben planificar sus importaciones teniendo en cuenta estos plazos. El re‑registro suele ser más rápido. Cómo los medicamentos no registrados evaden la aduana y llegan al mercado Hetq envió la lista de medicamentos no registrados y las direcciones de las farmacias al Comité de Ingresos del Estado, junto con los recibos fiscales. Tres de los medicamentos llevaban sellos fiscales, lo que significa que su venta se realizó dentro del marco fiscal legal a pesar de no estar registrados. Doce medicamentos vinieron con recibos que mostraban sus nombres de fármaco. Pedimos al SRC que explique: - Los casos de violaciones de las reglas de los recibos fiscales, especialmente la emisión de recibos sin documentos de compra; - Las razones de la ausencia de etiquetas de sello en algunos medicamentos; - La legalidad de la presencia o ausencia de etiquetas de sello en ciertos medicamentos. El SRC respondió que se realizaría una auditoría temática de impuestos y que se comunicarían los resultados, pero no se proporcionó un plazo. Mercado de alto riesgo, supervisión débil La circulación de medicamentos es monitoreada por la Inspección Estatal de Salud y Trabajo, que opera al servicio del Gobierno. Según la inspección, en 2024 inspeccionaron a 199 importadores y vendedores de medicamentos, emitieron 160 actos y aplicaron responsabilidad administrativa en 838 casos. Narek Karapetyan, jefe del Departamento de Circulación de Medicamentos de la Inspección, señala que se detectan medicamentos no registrados o importados ilegalmente, y se emiten órdenes de destrucción de las cantidades. Si el operador no cumple, sigue la responsabilidad administrativa. Además de las inspecciones planificadas, existe un mecanismo de compras de control. Por orden gubernamental, se realiza una compra de control bajo la directriz del jefe de la inspección, y una vez emitida la directriz, empieza la compra de control, seguida de una inspección. Cuando se le preguntó qué fundamentos justifican una compra de control — una queja, una sospecha o datos sospechosos — Karapetyan dijo que las compras de control se realizan únicamente dentro del marco de las inspecciones conforme a la ley. Si una organización figura en la lista de inspecciones anual, también puede estar sujeta a compras de control. Si llega información o una queja a la inspección, se abren procesos administrativos, se realizan inspecciones y, si es necesario, los medicamentos se remiten al centro de expertos para determinar si la importación y el registro se realizaron conforme a la ley. Las farmacias pagan multas y continúan vendiendo medicamentos no registrados. Si no hay queja o alerta, la supervisión puede repetirse al año siguiente, como máximo, si la empresa figura en la lista de inspección. En otras palabras, incluso tras las sanciones, un comerciante no queda impedido de seguir vendiendo un medicamento no registrado. Las acciones del Ministerio de Salud, de la Inspección y del Comité de Ingresos del Estado muestran que la supervisión de los medicamentos en el mercado es débil. Los tres principales organismos supervisores del sistema de salud prácticamente no cooperan de forma estrecha. Ese vacío permite que se vendan medicamentos no registrados libremente. Incluso después de las sanciones, las ventas no se detienen. Por lo tanto, el Estado debería encontrar una forma de registrar los medicamentos considerados esenciales para que las farmacias no violen las normas y los pacientes puedan usar medicamentos de calidad.